Kohlendioxid-Konzentration in Innenräumen
Einleitung
Ich habe vor einiger Zeit von
meinem Vater ein CO
2-Messgerät geschenkt bekommen. Ich hatte bisher keine Vorstellung davon, wie die CO
2-Konzentration in der Luft so ist und wie sie sich verändert. Ich war überrascht, wie schnell die Luftqualität in meinem Arbeitszimmer abnimmt! Misst das Ding überhaupt richtig?
Um das herauszufinden, muss ich wissen, wie viel Kohlendioxid ein Mensch (in dem Fall ich) in einer Stunde ausatmet und wie sich das auf die Kohlenstoffdioxid-Konzentration in einem geschlossenen Raum auswirkt.
Energieverbrauch
Die Menge ausgeatmeten CO2s hängt von der Menge Energie ab, die ein Mensch verbraucht. Kennt Ihr: fürs Treppensteigen braucht man mehr Energie als fürs Herumsitzen, und deswegen kommt man dabei leicht ins Schnaufen.
Wie viel Energie verbraucht ein Mensch, der Büroarbeit macht, in einer Stunde?
Dafür gibt es eine Faustregel: ein ruhender Mensch hat dieselbe Leistung wie eine helle altertümliche Glühbirne: 100W.
Da W = P * t, folgt: W = 100W * 3600s = 360kJ .
Genauerer Energieverbrauch
Man kann das auch genauer berechnen, laut
Wikipedia ist die folgende Abschätzung eine gute Näherung:
Grundumsatz eines Mannes = 105kJ pro Kilogramm Körpergewicht und Tag
Gesamter Energieumsatz bei Bürotätigkeit = Grundumsatz * 1.4
Gesamter Energieumsatz einer Frau = Umsatz eines Mannes * 0.9
Bei einer Frau mit dem Gewicht m sind das in einer Stunde:
Wh =
105 kJ kg-1 Tag-1 * m * 1.4 * 0.9
24 h Tag-1
Setzen wir m = 60kg, so folgt:
Wh ≈ 331kJ .
Das ist nah genug an der Abschätzung mit der Glühbirne.
Energiegewinnung aus Nahrung
So, und wie hängt diese Energiemenge mit der Menge CO2 zusammen?
Der Mensch, wie jedes andere Säugetier, nimmt Nahrung zu sich und gewinnt daraus Energie.
Nehmen wir mal der Einfachheit halber an, dass die Energie nur aus Zucker gewonnen wird. Habt Ihr heute Morgen schon Kaffee mit Zucker getrunken? Oder ein Marmeladen- oder Honigbrot gegessen? Also, passt doch.
Wie wir durch genaues Studium einer Packung Zucker herausfinden können, enthält Zucker pro 100g eine Energiemenge von 400kcal oder 1680kJ.
Um Wh = 331kJ zu erzeugen, muss jemand also
mZucker =
= 19.7 g Zucker verbrennen.
Wie aus Zucker CO2 wird
Zucker wird bei der Energiegewinnung in Wasser und CO2 umgewandelt, nach folgender Formel:
C6H12O6 + 6 O2 → 6 CO2 + 6 H2O;
Das geht natürlich nicht ganz so einfach, aber Ihr wollt wahrscheinlich nicht, dass ich den ganzen Zitronensäurezyklus hier auch noch erkläre, oder?
Aus jedem Zuckermolekül werden also 6 Moleküle Kohlenstoffdioxid.
Das Molekulargewicht von Zucker ist 6 * 12 + 12 * 1 + 6 * 16 g/mol = 180 g/mol .
1 Mol ist eine Menge von 6.022 * 1023Molekülen (Avogadro'sche Zahl).
Aus mZucker = 19.7g werden also
nZucker = 19.7 g / 180 g mol-1 = 0.11 mol .
und entsprechend 6 Mal so viel Mol CO2: nCO2 = 0.66 mol .
Anteil CO2 in der Luft
Luftmenge m Arbeitszimmer
Um berechnen zu können, wie stark der Kohlendioxidgehalt der Luft durch diese 0.66 mol steigt, muss ich wissen, wie viele Luftmoleküle insgesamt in meinem Arbeitszimmer sind. Denn die berühmten parts per million (ppm), in denen die Kohlenstoffdioxidkonzentration meist angegeben wird, bezieht sich auf den Volumenanteil, der in Gasen glücklicherweise identisch ist mit dem Anteil an Molekülen. Das Volumen einer bestimmten Anzahl an gasförmigen Molekülen ist nämlich unabhängig von der Größe, Form und Art der Teilchen. Es ändert sich allerdings mit Druck und/oder Temperatur. Das geht aus der allgemeinen Gasgleichung hervor:
p * V = n * R * T
(Druck * Volumen = Teilchenanzahl * allgemeine Gaskonstante * Temperatur)
daraus folgt
nZimmer =
Mein Arbeitszimmer hat eine Grundfläche von 4 * 3.2 m² und eine Höhe von 2.5 m, also ein Volumen von 32 m³.
Der Luftdruck ist bei durchschnittlichem Wetter auf Meereshöhe 1013mBar, was das gleiche ist wie 1013 Hektopascal oder 1.013 * 105 Pascal oder 1.013 * 105 N/m² .
Die Temperatur in meinem Zimmer ist, ich bin ja klimafreundlich und trage einen zweiten Pulli statt stark zu heizen, 19°C = 292 K.
Die allgemeine Gaskonstante ist R = 8.31 Nm mol-1 K-1
Daraus folgt:
nZimmer =
1.013 * 105 N/m² * 32 m³
8.31 Nm mol-1 K-1 * 292 K
= 1336 mol
CO2 Anteil
Wie oben berechnet atme ich in einer Stunde 0.66 mol CO2 aus.
Von den insgesamt vorhandenen 1336 mol sind das :
xCO2 = 0.66 / 1336 = 494 ppm.
Und, oh Wunder, das ist tatsächlich das, was in einer Stunde passiert: Die Anzeige des CO2-Messgerätes steigt innerhalb einer Stunde von morgendlichen, frisch gelüfteten ~500 ppm auf ungefähr 1000 ppm.
Lüften, lüften, lüften!
So, was lernen wir daraus? Laut Bundesumweltamt und anderen, internationalen Standards gilt eine Konzentration von 1400 ppm als "niedrige Luftqualität". Das würde ich also nach weniger als zwei Stunden erreichen.
Was bedeutet "niedrige Luftqualität" nun genau? Lebensgefährlich wird CO2 erst ab einer Konzentration von ca. 8%, das sind 80 000 ppm.
Wissenschaftler haben herausgefunden, dass die kognitive Leistungsfähigkeit von Menschen proportional mit zunehmender CO2 Konzentration abnimmt. Bei komplexen Aufgaben ist die Abnahme sogar noch stärker:
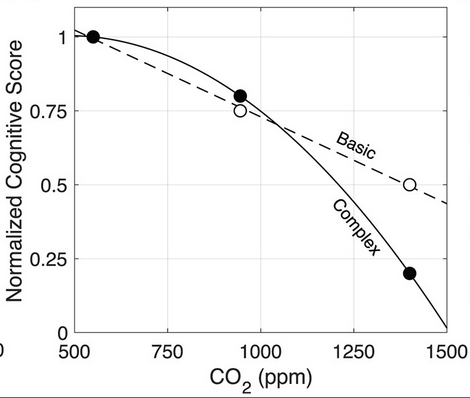
Quelle: Karnauskas et al., 2020.
Also, wenn jemand bei 1400 ppm nicht sofort lüftet, liegt das wohl daran, dass die verbleibenden 20% seiner geistigen Kapazität für so eine komplexe Aufgabe nicht mehr ausreichen 😉
Das CO2-Messgerät funktioniert jedenfalls richtig. Und das hätte ich wohl ohne Lüften nie herausfinden können.